
・アメリカスポーツ医学会認定運動生理学士
・株式会社フィットネス&コミュニティ代表
・プライベートジムBODY DIRECTOR代表
・YouTubeチャンネル
- ● 抗ヒスタミン薬(第一・第二世代)と認知症リスクの科学的知見
- ● 長期・高頻度使用が脳に与える影響とリスク上昇の条件
- ● 現時点で最もリスクが低いとされる具体的な花粉症薬の選び方
- ● 運動と腸内環境改善による「薬に頼らない体づくり」の重要性
目次
Toggle【免責事項】
本記事は医療アドバイスを提供するものではありません。著者はフィジカルコーチ(運動・身体管理の専門家)であり、医師・薬剤師ではありません。薬の変更・中止・継続については、必ずかかりつけの医師・薬剤師にご相談ください。本記事は公開されている研究論文をもとに情報提供を目的として執筆しています。
はじめに:「花粉症の薬で認知症になる」は正確か
「抗ヒスタミン薬を長く飲むと認知症リスクが上がる」 この情報を目にした方は多いかもしれません。
結論から言うと、現時点での研究が示すのは「一部の特定の薬を、非常に長期・高頻度で使い続けた場合にリスク上昇の関連が見られる」というものであり、「花粉症の薬一般が認知症の原因になる」とは言えません。
ただし科学の宿命として、「現時点での結論」は将来の研究によって変わる可能性があります。2024年に発表された研究では、これまでリスクが低いとされていた第二世代抗ヒスタミン薬でも、長期・高累積使用でリスク上昇を示す結果が出ており、専門家の間で活発に議論されています。
この記事では、現在何がわかっていて、何がまだわかっていないかを正確に整理します。そして「だからこそ薬に頼らない体をつくる」という積極的な選択肢を、フィジカルコーチとしてお伝えします。
まず知っておきたい:「第一世代」と「第二世代」の違い
抗ヒスタミン薬には2つの世代があります。リスクを理解するうえでこの違いが出発点になります。
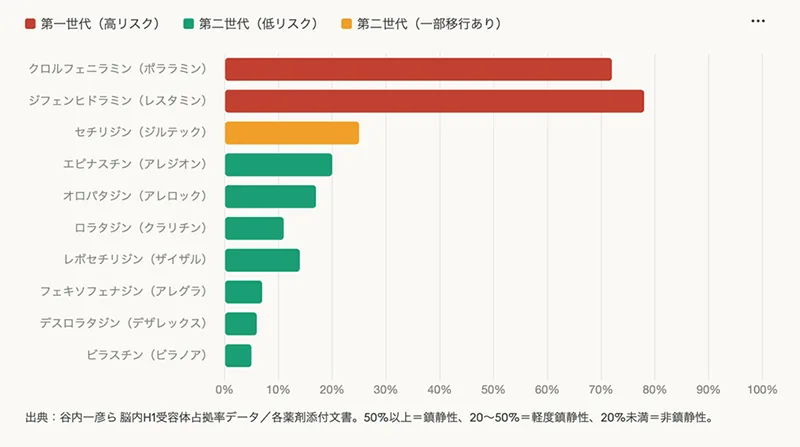
第一世代抗ヒスタミン薬(旧世代)
代表薬:ジフェンヒドラミン(レスタミン・ドリエル)、クロルフェニラミン(ポララミン)、クレマスチン(タベジール)
投与量の50%以上が脳内のH1受容体に結合し、強い眠気・鎮静作用が現れます。また「抗コリン作用」と呼ばれる副作用(口渇・便秘・認知機能低下)も強く、市販の風邪薬に多く含まれています。認知症リスクとの関連が複数の研究で示されているのは主にこの世代です。
第二世代抗ヒスタミン薬(現在主流)
代表薬:フェキソフェナジン(アレグラ)、ロラタジン(クラリチン)、ビラスチン(ビラノア)、デスロラタジン(デザレックス)、セチリジン(ジルテック)
血液脳関門を通過しにくく設計されており、脳内移行率20%以下が「非鎮静性」に分類されます。眠気・抗コリン作用が大幅に軽減され、現在の花粉症治療の主流です。
ただし第二世代でも「脳への移行がゼロ」ではなく、薬剤によって差があります。この点は後のセクションで詳しく整理します。
なぜ抗コリン薬が認知症リスクと関係するとされているのか
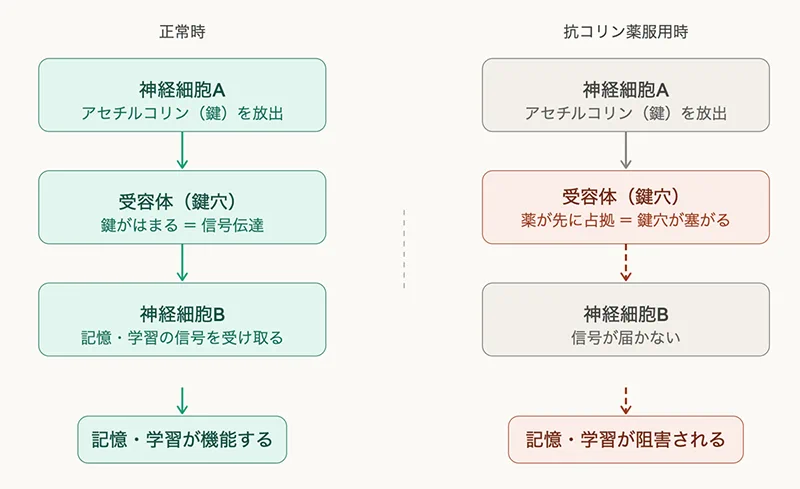
(図)アセチルコリンのメカニズム (正常時 vs 抗コリン薬服用時の対比)
「鍵と鍵穴」のイメージで理解する
脳内の神経伝達物質「アセチルコリン」は、記憶・学習・注意力の維持に中心的な役割を担っています。
神経細胞から放出されたアセチルコリン(鍵)が、隣の細胞の受容体(鍵穴)にはまることで、「覚える」「思い出す」という信号が伝わります。
抗コリン作用を持つ薬はこの「鍵穴」を物理的に塞ぎます。短期的には服用中の眠気や記憶のぼんやり感として現れ、薬が代謝・排泄されれば回復します。
問題になるとされているのは長期・高頻度の使用です。記憶と深く関わる脳の領域(特に海馬と大脳皮質)にはこの「鍵穴」が非常に多く存在しており、長年にわたって繰り返し塞がれ続けると、その経路自体が徐々に機能低下していく可能性が示されています。アルツハイマー病の脳ではアセチルコリンの量がもともと低下していることも知られており、これが「抗コリン薬の長期使用→認知症リスク上昇」という仮説の生物学的根拠です。
なお、薬そのものが体内に蓄積するわけではありません。抗コリン薬は服用後に肝臓で代謝され、通常数時間〜1日以内に血中から消失します。リスクとは「遮断されている時間の積み重ね」であり、毎日少量でも長期飲酒が肝臓に影響を与えるという構造に近いものです。
主要な論文・統計データ
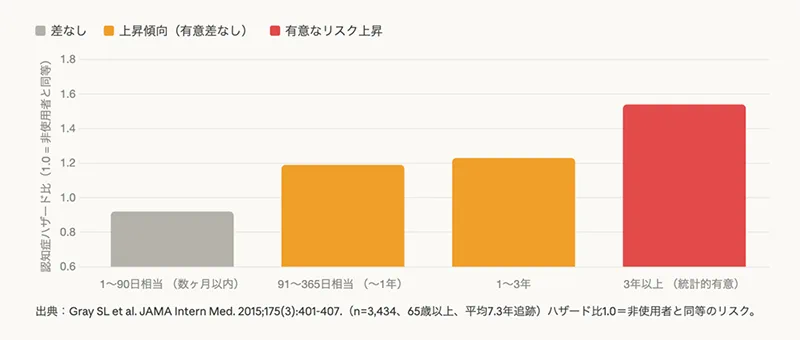
(図)累積服用量と認知症ハザード比 (Gray 2015 のデータ)
① Gray et al., 2015(JAMA Internal Medicine):第一世代を対象とした主要研究
ワシントン大学による3,434名・平均7.3年追跡の前向きコホート研究。対象は65歳以上の高齢者で、抗コリン作用の強い薬剤(第一世代抗ヒスタミン薬・三環系抗うつ薬・膀胱抗ムスカリン薬など)の累積使用量と認知症発症の関係を調査しました。
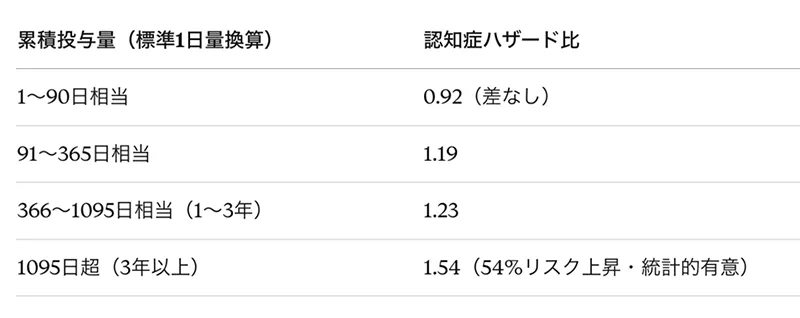
花粉シーズンのみの短期使用ではリスク上昇は見られず、「ほぼ毎日・3年以上」という高累積使用がリスク上昇の条件です。
出典:Gray SL et al. JAMA Intern Med. 2015;175(3):401-407. PMID: 25621434
② Coupland et al., 2019(JAMA Internal Medicine)
英国・55歳以上、認知症群58,769名 vs 対照群225,574名のネステッド症例対照研究。抗コリン性抗うつ薬・抗パーキンソン薬・膀胱抗ムスカリン薬などで有意なリスク上昇。リスクは診断の3〜16年前の暴露でも検出されており、逆の因果関係(認知症の前兆があるから薬が処方された)を排除した設計です。
出典:Coupland CAC et al. JAMA Intern Med. 2019;179(8):1084-1093.
③ Cochrane Review(系統的レビュー)
50歳以上を対象とした25研究(計968,428名)のまとめ。抗コリン認知的負担が高いと判定された場合、認知症リスクは2倍以上。ただし、因果関係の確定には更なる研究が必要と結論づけています。
④ Ancelin et al., 2006(BMJ)
抗コリン薬1年以上使用者の80%に軽度認知障害が確認(非使用者は35%)。対象が高齢者であること、服用中止で回復する例もあることを付記。
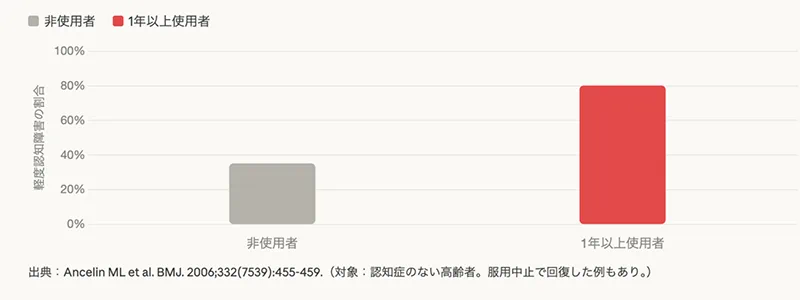
(図)非使用者35% vs 使用者80%の軽度認知障害比較 (Ancelin 2006)
⑤ 日本老年薬学会(2024年):日本版リスクスケール
「日本版抗コリン薬リスクスケール(第2版)」を策定。第一世代抗ヒスタミン薬を含む33薬剤がリスクスコア最高値(スコア3)に分類されています。
スコア3は「通常の服用量で脳内の鍵穴(ムスカリン受容体)を確実にブロックする強さ」を持つと判定された薬剤群を指します。スコア1・2と比較して認知機能への影響リスクが有意に高いとされています。
第二世代抗ヒスタミン薬のリスクは?——最新研究と残る不確実性
ここが、現時点で最も正直に伝えなければならない部分です。
従来の理解:第二世代は「ほぼ安全」
第二世代は血液脳関門を通過しにくく設計されており、脳内への移行を能動的に排除するP糖蛋白というポンプ機構も働いています。従来の研究では認知機能への影響はほぼ見られませんでした。
2024年・台湾大規模研究:予想外の結果
台湾の国民健康保険データベースを使い、アレルギー性鼻炎患者677,971名を対象とした2024年の研究(Su et al.)では、第二世代でも累積使用量に応じて認知症リスクが上昇するという結果が出ました。
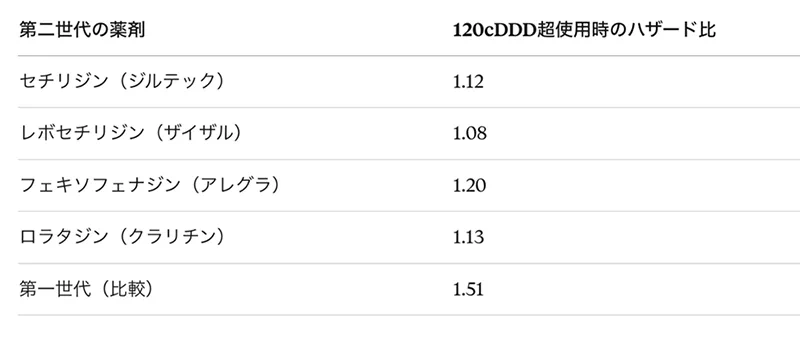
第一世代よりリスクは低いものの、第二世代も「ゼロではない」という結果です。
しかしこの研究には重要な反論がある
この結果を受け、アレルギー専門家から即座に反論が発表されました(Journal of Allergy and Clinical Immunology: In Practice, 2024)。
指摘の核心は「脳への移行がラジオラベル実験で確認されていないフェキソフェナジンでもリスク上昇が見られた点が生物学的に説明できない」というものです。つまり「アレルギー性鼻炎という病気自体が認知症リスクを高める可能性」「症状が重い患者ほど薬を多く使うため、病気の重症度が本当の原因かもしれない」という交絡因子の問題が未解決のままです。
現時点での正直な評価

この評価は「現時点での」ものです。2024年の台湾研究のように、今後の研究で新しい知見が出る可能性は常にあります。科学の結論は更新されるものであり、「現在最も安全とされる薬」が将来変わる可能性を排除できません。
研究の限界と、この情報を使う際の心構え
ここまで見てきた研究には、共通する重要な限界があります。
これらはいずれも観察研究です。「薬を使った人に認知症が多かった」という関連は示せても、「薬が認知症を引き起こした」という因果関係は証明できません。アレルギーという病気自体が炎症を通じて脳に影響する可能性、認知症の前段階に睡眠障害や不安が現れてその治療薬として抗コリン薬が処方されていた可能性など、交絡因子の問題は各研究で指摘されています。
Cochrane Reviewも「関連はあるが因果関係の確定には更なる研究が必要」と結論づけています。
つまり現時点でのメッセージは「過度に恐れる必要はないが、不必要な長期・高累積使用は避けるのが合理的である」というものです。
では私たちは何をすべきか 安易に薬に頼らない体をつくる
研究の結論が将来変わる可能性がある以上、最も合理的な方針は「できるだけ薬を必要としない体をつくること」です。これはリスクを「ゼロにする」という話ではなく、「薬に頼る場面を減らす」という積極的な選択です。
花粉症はアレルギー性の免疫過剰反応です。同じ花粉量でも症状の出方に大きな個人差があるのは、免疫の調節力・腸内環境・慢性炎症の状態といった「体の土台」が異なるからです。この土台に直接働きかけられる手段のひとつが、運動と腸内環境の改善です。
腸内環境と花粉症の関係
腸内細菌叢はアレルギー反応を制御するTh1/Th2バランスに深く関与しています。腸内環境が乱れると免疫過剰反応が起きやすくなり、花粉症が悪化しやすくなることが報告されています。食物繊維・発酵食品の摂取、過度な抗菌薬使用の回避などが腸内環境の改善につながります。腸内環境の改善は、花粉症の症状軽減と同時に、全身の慢性炎症の軽減を通じて認知機能保護にも寄与する可能性が研究で示されています。
運動という最も有力な答え
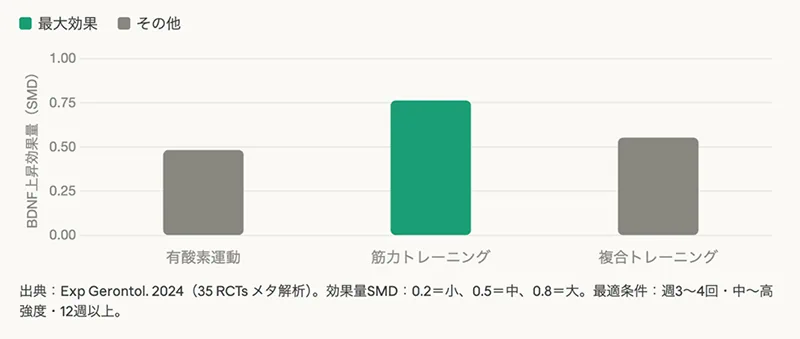
(図)運動種別のBDNF上昇効果量 (35 RCTs メタ解析)
運動は、花粉症の症状軽減と認知症リスク低下の両方に、直接働きかけることができる唯一の手段です。
花粉症の症状に対する効果
有酸素運動(8週間・週3回・最大心拍数65〜70%)を行った花粉症患者では、鼻炎症状スコアが有意に低下し、炎症性サイトカイン(IL-4)も減少したことがRCTで確認されています。筋力トレーニング(6ヶ月)でも、鼻・目の症状スコア・生活の質・血中炎症マーカー(IL-4、IL-6、IgE)がいずれも有意に改善(p<0.05)しました。
参照:Asian Pac J Allergy Immunol. 2018 / Ann Allergy Asthma Immunol. 2025
認知症リスクに対する効果
骨格筋は「動く器官」であると同時に、脳と双方向にコミュニケーションする内分泌器官です。筋肉が収縮すると、脳の神経保護に直接関与するBDNF(脳由来神経栄養因子)をはじめとする因子が放出されます。
35のRCTを統合したメタ解析では、BDNF上昇効果は有酸素運動SMD=0.48・筋力トレーニングSMD=0.76・複合トレーニングSMD=0.55であり、筋力トレーニングが最大値を示しています。最も効果が高かった条件は「週3〜4回・中〜高強度・12週以上」です。
参照:Exercise training alters resting BDNF in older adults. Exp Gerontol. 2024.(35 RCTs)
一本の線でつながっている
運動 → 花粉症の症状が和らぐ → 服薬量・服薬期間が減る → 抗コリン負荷が下がる → 認知症リスクが下がる。そしてその運動自体が、認知症リスクをさらに直接下げる。
薬のリスクについての研究がどのように更新されても、「運動と腸内環境を整えることで薬に頼らない体をつくる」という方向性は、どんな結論にも対応できる最も合理的な選択です。
まとめ
現時点でわかっていること:
- ・第一世代抗ヒスタミン薬の「ほぼ毎日・3年以上」の高累積使用では、認知症リスク上昇の関連が複数の研究で示されている
- ・花粉シーズンのみの短期使用ではリスク上昇は確認されていない
- ・第二世代については2024年の研究で弱い関連が示されたが、因果関係は未確定で専門家の間でも議論中
- ・フェキソフェナジン・ビラスチン・デスロラタジンは現時点で最も脳への影響が少ないとされる
現時点でわかっていないこと:
- ・第二世代の長期使用リスクについての確定的な結論
- ・アレルギーという病気自体と認知症の関係の切り分け
- ・研究結果が将来どう更新されるか
今できること:
- ・薬に頼らない体をつくる(運動・腸内環境の改善)
- ・薬を使う際は第二世代の非鎮静性薬剤を選ぶ
- ・不必要な長期・高累積使用は避ける
- ・疑問があれば医師・薬剤師に相談する
参考文献
- 1. Gray SL, et al. Cumulative use of strong anticholinergics and incident dementia. JAMA Intern Med. 2015;175(3):401-407. PMID: 25621434
- 2. Coupland CAC, et al. Anticholinergic drug exposure and the risk of dementia. JAMA Intern Med. 2019;179(8):1084-1093.
- 3. Ancelin ML, et al. Non-degenerative mild cognitive impairment and use of anticholinergic drugs. BMJ. 2006;332(7539):455-459.
- 4. Cochrane Review: Anticholinergic drugs and risk of dementia (CD013540). 50歳以上968,428名・25研究
- 5. 日本老年薬学会「日本版抗コリン薬リスクスケール(第2版)」2024年5月
- 6. Su CH, et al. Cumulative dose effects of H1 antihistamine use on the risk of dementia in patients with allergic rhinitis. J Allergy Clin Immunol Pract. 2024;12:2155-2165.
- 7. Kumar et al. Correlation, causation, and confounding: how worried should we be about dementia risk and second-generation antihistamines? J Allergy Clin Immunol Pract. 2024.
- 8. Exercise training alters resting BDNF in older adults: systematic review with meta-analysis. Exp Gerontol. 2024.(35 RCTs)
- 9. Physical Activity to Counter Age-Related Cognitive Decline. Sports Med Open. 2025.
- 10. Asian Pac J Allergy Immunol. 2018 / Ann Allergy Asthma Immunol. 2025(運動と花粉症症状改善)
本記事は情報提供を目的としており、医療アドバイスではありません。薬に関する判断は必ず医療専門家にご相談ください。

